VIDAS® HIV Panel
Frühzeitige Diagnostik durch fortschrittliche Tests der 4. Generation
Das VIDAS® HIV Panel umfasst eine Zusammenstellung der modernsten Tests der 4. Generation und liefert einen verbesserten Nachweis einer akuten HIV-Infektion während des kritischen “Zeitfensters”.
- Kombinierter Nachweis von Anti-HIV-1 (Gruppe M und O) und Anti-HIV-2 Gesamtimmunglobuline + HIV-1 p24-Antigen
- Zweifachinformation: Abgrenzung von Ag- und Ab-Signalen
- Höchste derzeit erreichbare p24 Ag-Sensitivität
- Anwenderfreundliche Lösung
Benötigen Sie weitere Informationen?
Viele der 35,3 Millionen HIV-Infizierten weltweit wissen nichts von ihrer Erkrankung, weil Krankheitssymptome fehlen oder unspezifisch sind. Außerdem können zwischen dem Zeitpunkt der Kontamination und dem Auftreten der ersten Anti-HIV-Serumantikörper durchschnittlich 3 Wochen liegen1. Der frühzeitige Nachweis einer Serokonversion ist deshalb eine der größten Herausforderungen in der HIV-Diagnostik.
Die automatisierten VIDAS® HIV-Screeningtests ermöglichen den gleichzeitigen Nachweis des p24-Antigens und der Anti-HIV-Antikörper, so dass sich die Zeitspanne zwischen der Kontamination und der Diagnose verringert. Die Identifizierung weiterer Primärinfektionen kann wesentlich zur Verringerung der Übertragungsrate beitragen. Für die Verbesserung der Lebensqualität der Patienten ist es ebenso wichtig, so schnell wie möglich eine angemessene Therapie einzuleiten.
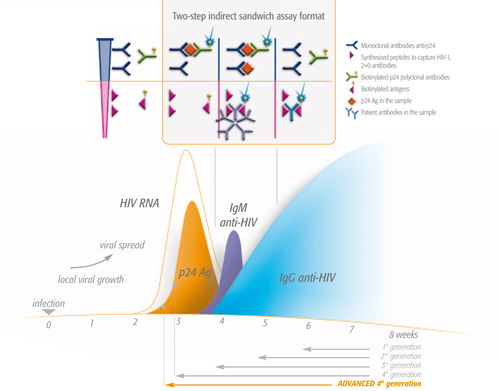
Einzigartiges Testprinzip
VIDAS® HIV Panel:

Testprinzip:
Ausgezeichnete Leistungsdaten
- Beste analytische Sensitivität verglichen mit anderen häufig verwendeten Tests2,3
- Niedrigste Nachweisgrenze für HIV-Infektionstests2,3
- Höchste derzeit erreichbare Sensitivität gegenüber p24 Ag (niedrigere Nachweisgrenze gemessen am WHO-Standard):
- VIDAS® HIV Duo Ultra: 0,66 IU/ml3
- VIDAS® HIV Duo Quick: 0,43 IU/ml3
- VIDAS® HIV P24: 0,73 - 1,15 IU/ml3
Anwenderfreundlichkeit und Flexibilität für Ihr Labor
- Anwenderfreundliche Testkonzeption
- Ein Teststreifen pro Patient
- VIDAS® steht für Robustheit und Zuverlässigkeit
Referenzen:
- Kleinman S., et al. Transfusion Medicine Reviews. July 1997. Vol. 11, N° 3 p. 155-172.
- Ly TD, et al. 2007 Jul; 143(1):86-94. Epub 2007 Mar 28.
- Miedouge M, et al. J Clin Virol. 2011 Jan;50(1):57-60. doi: 10.1016/j.jcv.2010.09.003.
| VIDAS® HIV DUO Ultra |
VIDAS® HIV DUO Quick |
VIDAS® P24 II | |
|---|---|---|---|
| Bestellnummer | 30443 | 30447 | 30117 |
| Tests/Kit | 60 | 60 | 30 |
| Probenmaterial | Serum oder Lithium-Heparin-Plasma oder EDTA-Plasma | ||
| Probenvolumen | 200 µL | ||
| Kalibrier- & Regel-stabilität | 14 Tage | ||
| Ergebnisse | Getrennte Ergebnisse für Ag und Ab |
Gesamtergebnis | |
| Sensitivität in Ag | 11.5 pg/ml HIV Ag | 16.5 pg/ml HIV Ag | 11.25 pg/ml HIV Ag |
| VIDAS® HIV P24 II Bestätigung | |
|---|---|
| Bestellnummer | 30 444 |
| Tests/Kit | 60 Tests |
Weitere technische Angaben finden Sie auf www.myvidas.com.
Ähnliche Publikationen
- Ly TD, Ebel A, Faucher V, Fihman V, Laperche S. Could the new HIV combined p24 antigen and antibody assays replace p24 antigen specific assays? J Virol Methods. 2007 Jul;143(1):86-94. Epub 2007 Mar 28.
- Miedouge M, Grèze M, Bailly A, Izopet J. Analytical sensitivity of four HIV combined antigen/antibody assays using the p24 WHO standard. J Clin Virol. 2011 Jan;50(1):57-60. doi: 10.1016/j.jcv.2010.09.003.
Richtlinien
- World Health Organization
- Guidance on provider-initiated HIV testing and counselling in health facilities
- Delivering HIV test results and messages for re-testing and counselling in adults
Weitere wissenschaftliche Quellen finden Sie auf www.myvidas.com.